Une maladie ultra-rare à pronostic sévère
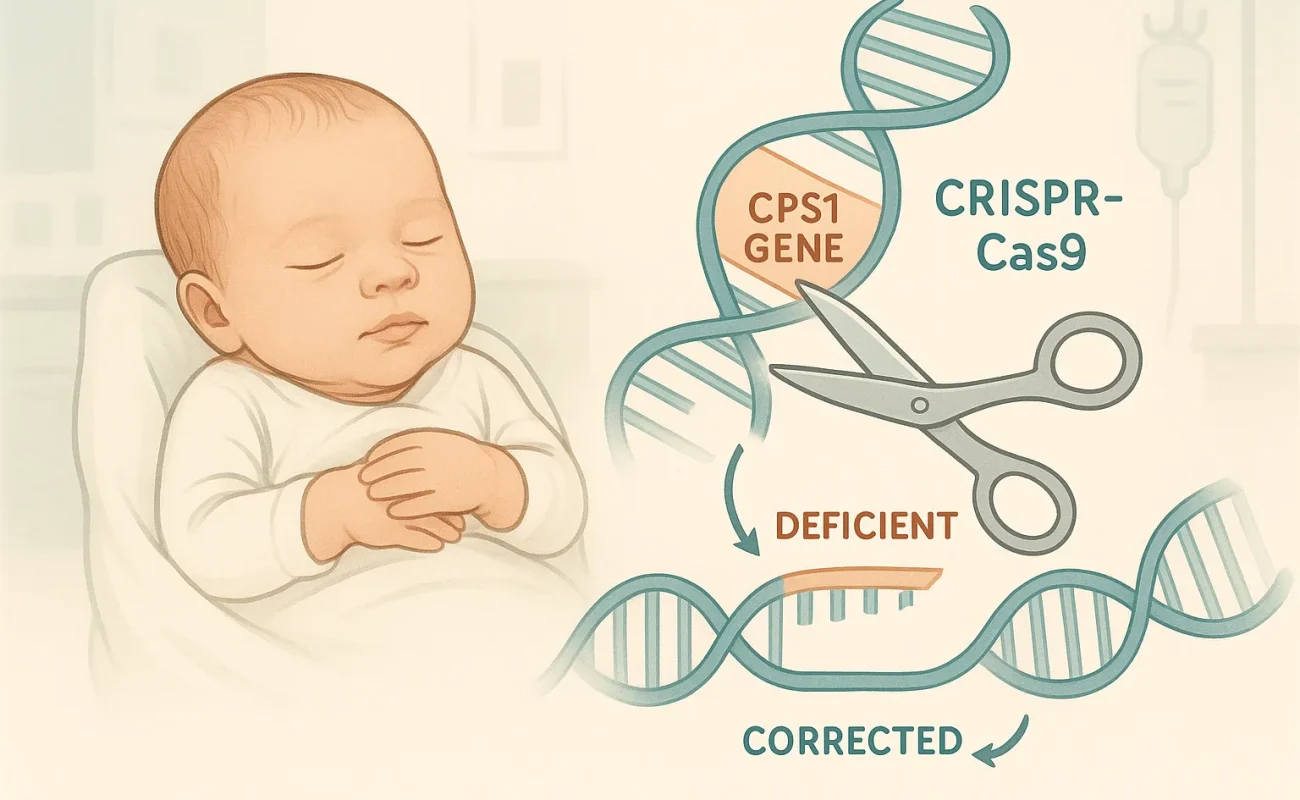
Le déficit en CPS1 est une maladie génétique ultra-rare, avec une incidence estimée à environ 1 cas pour 800 000 naissances vivantes. Cette pathologie métabolique grave se manifeste dès la petite enfance par une accumulation toxique d’ammoniaque dans le sang (hyperammoniémie), pouvant entraîner coma, lésions cérébrales irréversibles et mortalité néonatale élevée. Sans traitement curatif, la mortalité atteint 70 à 80% dans les premiers mois, et les survivants présentent souvent des séquelles neurologiques sévères.
Une avancée majeure dans le traitement d’une maladie métabolique rare
Pour la première fois, un nourrisson atteint de cette pathologie a bénéficié d’une thérapie génique personnalisée utilisant l’édition de base CRISPR-Cas9. La maladie est causée par deux variants tronqués du gène CPS1, identifiés comme Q335X paternel et E714X maternel, responsables du défaut enzymatique.
Stratégie d’édition précise via base editing
Le traitement repose sur une édition de base visant la conversion ponctuelle d’une seule base (mutation A>G), évitant les cassures de l’ADN double brin et la complexité des oligonucleotides simple brin (ssODN). Cette méthode limite significativement les risques d’effets hors cible et accroît la sécurité du procédé.
Livraison ciblée par nanoparticules lipidiques (LNP)
La plateforme thérapeutique utilise des nanoparticules lipidiques pour délivrer simultanément l’ARNm codant pour Cas9 et les ARN guides spécifiques aux cellules hépatiques, garantissant excellente spécificité tissulaire, faible immunogénicité et possibilité d’administrations répétées en toute sécurité.
Rapidité de développement et succès clinique
La thérapie, conçue et validée en seulement six mois, a été administrée sans effets secondaires graves. Le suivi clinique montre une correction génomique efficace et durable, offrant un espoir inédit pour les maladies rares dépourvues de traitements adaptés.
Vers une médecine génomique personnalisée et agile
Cette réalisation marque une étape cruciale vers une médecine personnalisée capable de répondre rapidement aux besoins des patients atteints de maladies génétiques rares. Elle illustre la maturité technologique des outils CRISPR-Cas9 associés à des systèmes de délivrance avancés, confirmant l’essor de thérapies géniques modulables et sécurisées pour les maladies métaboliques complexes.
Sources :
NIH News Release – Infant with rare, incurable disease is first to successfully receive personalized gene therapy treatment
https://www.nih.gov/news-events/news-releases/infant-rare-incurable-disease-first-successfully-receive-personalized-gene-therapy-treatment
Children’s Hospital of Philadelphia – World’s First Patient Treated with Personalized CRISPR Gene Editing Therapy
https://www.chop.edu/news/worlds-first-patient-treated-personalized-crispr-gene-editing-therapy-childrens-hospital
Le Monde – Un nourrisson atteint d’une maladie génétique ultra-rare reçoit un traitement personnalisé inédit
https://www.lemonde.fr/realites-biomedicales/article/2025/05/17/un-nourrisson-atteint-d-une-maladie-genetique-ultra-rare-recoit-un-traitement-personnalise-inedit_6606541_6579630.html